4月25日,我院在国家药物和医疗器械临床试验机构备案管理信息系统中完成了药物临床试验机构备案,备案号为“药临床机构备字2021000058”。此次备案了胃肠外科、消化内科、肾病学、免疫学、神经内科、肿瘤科、血液内科、心血管内科共计8个专业,标志着我院可在备案专业内开展药物Ⅱ、Ⅲ期以及上市后再评价的Ⅳ期临床试验项目。至此,在我院去年取得“医疗器械临床试验机构”的基础上,又新增了一个国家级临床科研平台,助力我院推进高水平医院建设任务。
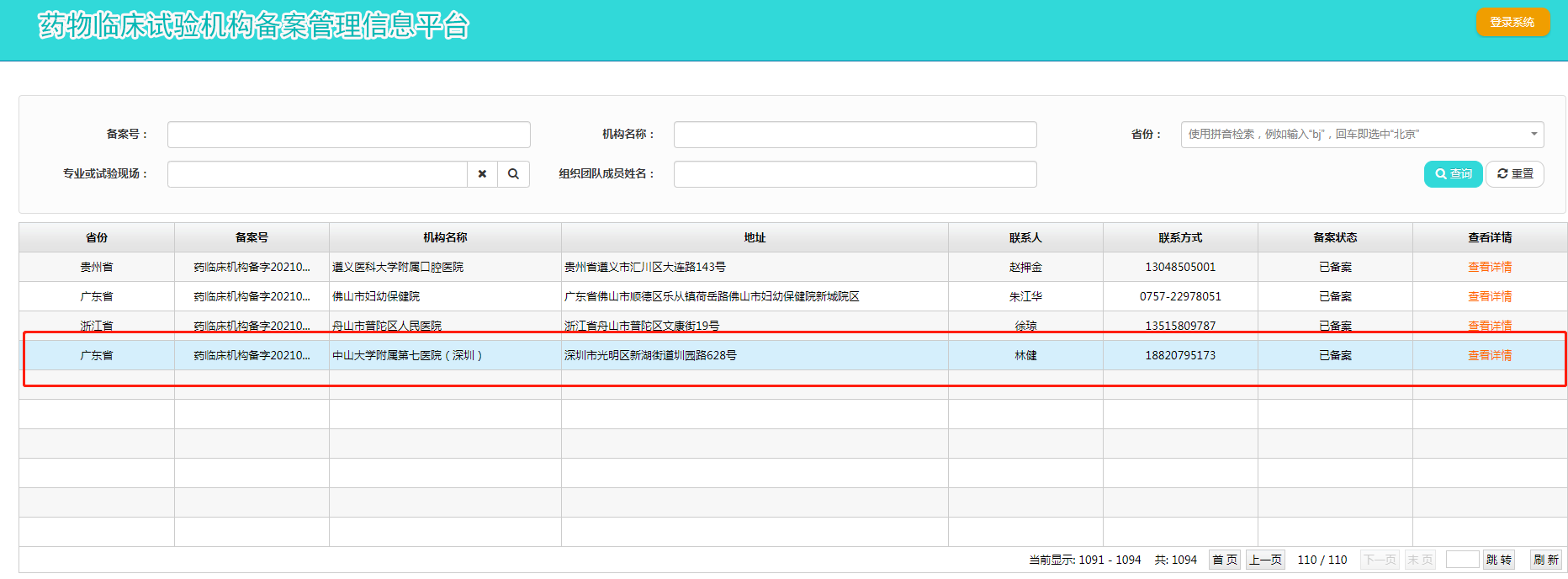
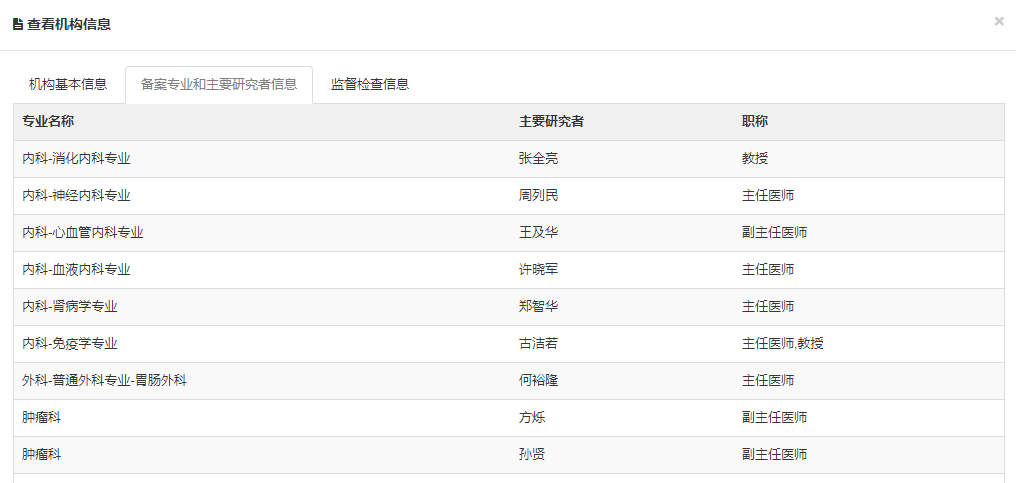
国家药监局备案系统信息
为了提高医院医疗和科研学术水平,我院于 2020 年1月开始筹建药物临床试验机构,院领导对此项工作高度重视并给予了大力支持,迅速健全了组织架构,成立了药物临床试验机构。机构成立后,机构办公室在临床医学研究中心的统一领导下,完善了备案注册资料,制定了规范的药物临床试验文件管理制度。在医院的大力支持下,机构配套设置了与药物临床试验相适应的办公场所、临床试验药房、资料档案室,以及必要的设备设施。2020年6月,机构办公室组织举办了省级药物临床试验质量管理规范(GCP)培训班 ,使全院391人获得了GCP证书,从而为机构及相关专业的顺利备案打下了基础。

GCP培训班
为完善我院药物临床试验机构备案工作,顺利迎接省药监局对新备案机构的常规例行检查,备案前,我院委托广东省药学会药物临床试验专业委员会对我院进行了第三方评估。评估专家组听取了相关工作汇报,对我院药物临床试验机构、伦理委员会以及8个拟申报的临床专业科室和辅助科室的文件管理制度、培训记录、人员资格证书及设施设备的配置进行了现场检查,同时对机构办、伦理委员会和临床专业的相关人员进行了现场提问。

第三方评估检查
经过两轮严格的现场检查和提问考核,检查专家对我院药物临床试验机构的筹备建设和管理给予了充分肯定,认可我院已符合药物临床试验机构的备案条件,同时对我院目前药物临床试验建设中存在的问题也提出了进一步完善的意见及建议,并形成了第三方评估报告,为今后我院开展药物临床试验工作提出了宝贵的指导性意见。

我院第三方评估报告
我院国家药物临床试验机构的成功备案,为我院开展注册类药物临床试验提供了创新平台,对促进医院临床研究的科学性和规范化,打造研究型、创新型医院,以及加快医院健康快速发展具有重要意义。我院药物临床试验机构办公室将进一步抓紧落实GCP相关培训,对在研项目把好质量关,并加强受试者权益保护意识,以保证临床试验项目的顺利开展。同时,机构办公室也会做好各项准备,迎接药品监督管理部门、卫生健康主管部门对新备案机构的监督检查。



